Фазовые диаграммы. Диаграмма фазовых состояний многокомпонентной системы Фазовая диаграмма воды
Читайте также
Однокомпонентные системы. Однокомпонентной системой является любое простое в-во или хим. соед., обладающее строго определенным составом в газообразном, жидком и твердом состояниях. Диаграммы состояния обычно строят на плоскости в координатах Т-р (рис. 1). Фазовые поля (области существования) пара V, жидкости L и твердой фазы S дивариантны, т.е. допускают одновременное изменение двух параметров состояния - Т и р.
Рис. 1 Диаграмма состояния однокомпонентной системы. S, L и V - соотв. области существования твердой, жидкой и паровой фаз; 1, 2 и 3 кривые кипения (испарения), плавления и возгонки (сублимации) соотв., К критич. точка; А тройная точка .
Обычно при повышении т-ры взаимная растворимость жидкостей увеличивается, поэтому по своим св-вам оба насыщенных р-ра, составы к-рых изменяются по отрезкам бинодали ЕК и KF, сближаются. Наконец, при т-ре T к различие между ними исчезает; эта т-ра наз. критической т-рой растворимости (смешения), выше нее может существовать лишь одна жидкая фаза. Большинство систем с расслоением р-ров характеризуются только одной критич. т-рой р-римости, чаще всего верхней, т. е. на диаграмме состояния имеют незамкнутую снизу бинодаль. Если в таких системах не образуются хим. соед., область сосуществования двух жидких фаз ограничена снизу кривой кристаллизации одного из компонентов при т-ре превращения жидкая фаза 1
D
жидкая фаза 2 + твердая фаза. Такое трехфазное равновесие наз. монотектическим; оно по своей термодинамич. природе аналогично эвтектическому или эвтектоидному. При синтектическом трехфазном равновесии две жидкие фазы взаимодействуют с образованием твердого соед. Такое равновесие аналогично перитектическому.
В нек-рых системах бинодаль имеет форму замкнутой кривой (овал), т. е. система имеет две т-ры смешения верхнюю и нижнюю.
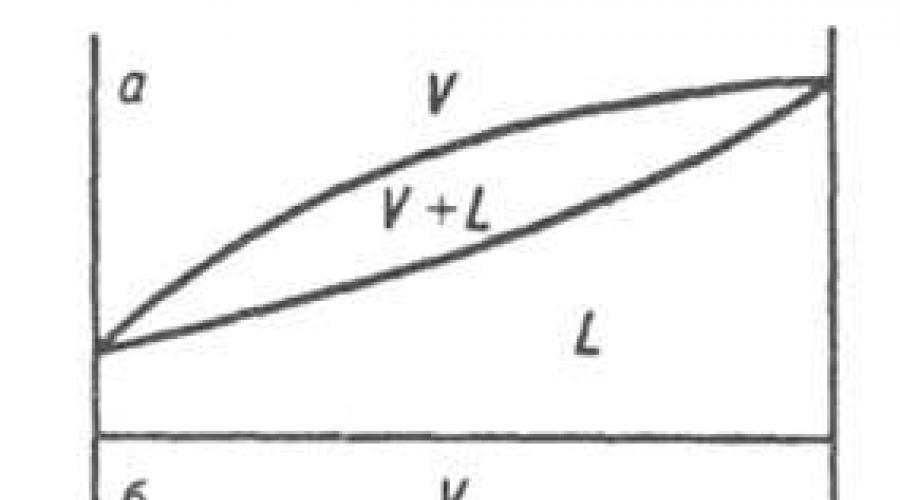
Диаграмма равновесия жидкость-пар. При р = const каждому составу жидкой смеси отвечает определенная т-ра равновесия с паром и определенный состав пара , отличающийся, как правило, от состава жидкой смеси . На диаграмме состояния (рис. 8, а) кривые кипения и конденсации изображают зависимости т-р начала кипения и конденсации от состава и отделяют поля жидкости L и пара V от поля (L + V)гетерог. состояний жидкость-пар. На кривой кипения м. б. экстремум: максимум (рис. 8, б) или минимум (рис. 8, в); в этих точках кривая кипения касается кривой конденсации , т. е. составы равновесных жидкости и пара совпадают Жидкие смеси такого состава полностью выкипают, подобно чистым жидкостям , при постоянной т-ре без изменения состава (см. Азеотропные смеси). Диаграммы состояния, описывающие равновесия двухкомпонентных твердых р-ров с жидкими р-рами и жидких р-ров с паром , подобны.

Рис. 8. Диаграммы состояния, двойной системы, описывающие равновесие жидкость - пар . L и V области существования жидкости и пара соотв.. (L + V) область сосуществования жидкой и паровой фаз; а система без азеотропной точки; б и в два типа азеотропных смесей
Тройные системы. Состояния тройных систем однозначно определяются четырьмя независимыми параметрами: Т, р и молярными (массовыми) долями двух компонентов (доля третьего компонента определяется из условия равенства единице суммы долей всех компонентов). Поэтому при построении диаграмм состояния тройных систем один из независимых параметров (р или Т) или два (р и T) фиксируют и рассматривают пространственные изобарные или изотермич. диаграммы или плоские изобарно-изотермич. диаграммы, соответствующие одному из сечений пространственной диаграммы состояния. Каждому составу тройной смеси отвечает определенная точка на плоскости составов. Область возможных составов тройных систем наз. композиционным треугольником или треугольником составов. В системе прямоугольных координат он представляет собой прямоугольный равнобедренный треугольник, вершины к-рого отвечают компонентам А, В и С, а стороны - двойным смесям АВ, ВС и СА. Более распространено использование равностороннего композиц. треугольника. В этом случае все компоненты равноправны, а за начало координат можно с равным основанием принять любую из его вершин (см. Многокомпонентные системы). Для построения пространств. изобарной или изотермич. диаграммы состояния по координатной оси, перпендикулярной композиц. треугольнику, откладывают соотв. T или р. При этом фигуративные точки системы в целом и ее трехкомпонентных фаз оказываются расположенными внутри трехгранной призмы, грани к-рой изображают двойные системы, ребра -однокомпонентные системы. На рис. 9, а изображена простейшая
Фазой называется термодинамическое равновесное состояние вещества, отличающееся по физическим свойствам от других возможных равновесных состояний того же вещества. Переход вещества из одной фазы в другую – фазовый переход - всегда связан с качественными изменениями свойств тела. Примером фазовых переходов могут служить изменения агрегатного состояния. Но понятие «фазовый переход» шире, т.к. оно включает и переход вещества из одной модификации в другую при сохранении агрегатного состояния (полиморфизм), например, превращение алмаза в графит.
Различают два вида фазовых переходов:
Фазовый переход 1 рода – сопровождается поглощением или выделением теплоты, изменением объема и протекает при постоянной температуре. Примеры: плавление, кристаллизация, испарение, сублимация (возгонка) и др.
Фазовые переходы 2 рода – протекают без выделения или поглощения тепла, с сохранением величины объема, но скачкообразным изменением теплоемкости. Примеры: переход ферромагнитных минералов при определенных значениях давления и температуры в парамагнитное состояние (железо, никель); переход некоторых металлов и сплавов при температуре близкой к 0 0 К в сверхпроводящее состояние (ρ = 0 Ом∙м) и др.
Для химически однородного вещества понятие фазы совпадает с понятием агрегатное состояние. Рассмотрим для такой системы фазовые превращения, используя для наглядности диаграмму состояния. На ней в координатах р и Т задается зависимость между температурами фазовых переходов и давлением. Эти зависимости в виде кривых испарения (ОИ), плавления (ОП) и сублимации (ОС) и образуют диаграмму состояния.
Точка О пересечения кривых определяет условия (значения Т и р), при которых все три агрегатные состояния вещества находятся в термодинамическом равновесии.
По этой причине она называется тройной точкой. Например, тройная точка воды является одной из реперных точек температурной шкалы Цельсия (0 0 С). Как следует из уравнения Клапейрона – Клаузиуса характер зависимости Т =f(р) для перехода твердое тело – жидкость (кривые ОП) может быть разным: Если вещество при переходе в жидкую фазу увеличивает объем (вода, висмут, германий, чугун …), то ход этой зависимости представлен на рис. 2а. Для веществ, уменьшающих объём при переходе в жидкую фазу, зависимость имеет вид показанный на рис. 2б.
Кривая испарения заканчивается критической точкой – К . Как видно из диаграммы, существует возможность непрерывного перехода жидкости в газообразную фазу без пересечения кривой испарения, т.е. без присущих такому переходу фазовых превращений.
При давлении меньшим, чем р тр.тчк. , вещество может существовать только в двух фазах: твердой и газообразной. Причем, при температурах, меньших Т тр.тчк. , возможен переход из твердого состояния в газ минуя жидкую фазу. Такой процесс называется сублимацией или возгонкой. Удельная теплота сублимации
τ суб = λ пл +r исп
ТВЕРДЫЕ ТЕЛА.
Твердое тело, агрегатное состояние вещества, для которого характерно наличие значительных сил межмолекулярного взаимодействия, стабильность формы и объема. Тепловое движение частиц твердого тела представляет собой небольшие по амплитуде колебания около положений равновесия. Различают кристаллическое и аморфное строение твердых тел.
Характерной особенностью микроструктуры кристаллов является пространственная периодичность их внутренних электрических полей и повторяемость в расположении кристаллообразующих частиц – атомов, ионов и молекул (дальний порядок). Частицы чередуются в определенном порядке вдоль прямых линий, которые называются узловыми. В любом плоском сечении кристалла две пересекающихся системы таких линий образуют совокупность совершенно одинаковых параллелограммов, которые плотно, без зазоров покрывают плоскость сечения. В пространстве пересечение трех некомпланарных систем таких линий образует пространственную сетку, которая разбивает кристалл на совокупность совершенно одинаковых параллелепипедов. Точки пересечения линий, образующих кристаллическую решетку называются узлами. Расстояния между узлами вдоль какого-то направления называется трансляциями или периодами решетки. Параллелепипед, построенный на трех некомпланарных трансляциях, называется элементарной ячейкой или параллелепипедом повторяемости решетки. Важнейшим геометрическим свойством кристаллических решеток является симметрия в расположении частиц по отношению к определенным направлениям и плоскостям. По этой причине, хотя и существует несколько способов выбора элементарной ячейки, для данной кристаллической структуры, выбирают ее так, чтобы она соответствовала симметрии решетки.
Существует два признака, по которым классифицируются кристаллы: а) кристаллографический – по геометрии кристаллической решетки и б) физический – по характеру взаимодействия частиц, расположенных в узлах кристаллической решетки и их природе.
Геометрия кристаллических решеток и их элементарных ячеек определяется количеством элементов симметрии, использованных при построении данной решетки. Число возможных видов симметрии ограничено. Русский кристаллограф Е.С. Федоров (1853 – 1919) показал, что существует всего 230 возможных комбинаций элементов симметрии, которые путем параллельного переноса, отражения и вращения обеспечивают плотную, т.е. без зазоров и щелей упаковку элементарных ячеек в пространстве. Браве показал, что существует всего 14 типов решеток, которые различаются по виду переносной симметрии. Различают примитивные (простые), базоцентрированные, обьемноцентрированные и гранецентрированные решетки Браве. По форме ячейки в зависимости от углов между ее гранями α, β и γ и соотношением между длиной ребер а, б и с эти 14 типов решеток образуют семь кристаллических систем (сингоний): кубическую, гексогональную, тетрагональную, тригональную или ромбоэдрическую, ромбическую, моноклинную и тригональную.
По характеру взаимодействия частиц, расположенных в узлах кристаллической решетки и их природе кристаллы делятся на четыре типа: ионные, атомные, металлические и молекулярные
Ионные – в узлах кристаллической решетки располагаются ионы противоположных знаков; взаимодействие обусловлено электростатическими силами притяжения (ионная или гетерополярная связь).
Атомные – в узлах кристаллической решетки располагаются нейтральные атомы, удерживающиеся в узлах гомеополярными, или ковалентными связями.
Металлические – в узлах кристаллической решетки располагаются положительные ионы металла; свободные электроны образуют, так называемый, электронный газ, который и обеспечивает связь ионов.
Молекулярные – в узлах кристаллической решетки располагаются нейтральные молекулы, силы взаимодействия между которыми обусловлены незначительным смещением электронного облака атома (поляризационные или ван-дер-ваальсовские силы).
Кристаллические тела можно разделить на две группы: монокристаллы и поликристаллы. Для монокристаллов наблюдается единая кристаллическая решетка в объеме всего тела. И хотя внешняя форма монокристаллов одного вида может быть разной, углы между соответствующими гранями будут всегда одинаковыми. Характерной особенностью монокристаллов является анизотропия механических, тепловых, электрических, оптических и др. свойств.
Монокристаллы нередко встречаются в естественном состоянии в природе. Например, большинство минералов – хрусталь, изумруды, рубины. В настоящее время в производственных целях многие монокристаллы выращивают искусственно из растворов и расплавов - рубины, германий, кремний, арсенид галия.
Один и тот же химический элемент может образовать несколько, отличающихся по геометрии, кристаллических структур. Это явление получило название - полиморфизма. Например, углерод – графит и алмаз; лед пять модификаций и др.
Правильная внешняя огранка и анизотропия свойств, как правило, не проявляются для кристаллических тел. Это объясняется тем, что кристаллические твердые тела обычно состоят из множества беспорядочно ориентированных мелких кристалликов. Такие твердые тела называются поликристаллическими. Связано это с механизмом кристаллизации: при достижении необходимых для этого процесса условий, очаги кристаллизации одновременно возникают во множестве мест исходной фазы. Зародившиеся кристаллы расположены и ориентированы друг по отношению к другу совершенно хаотически. По этой причине по окончании процесса мы получаем твердое тело в виде конгломерата сросшихся мелких кристалликов – кристаллитов.
ДЕФФЕКТЫ В КРИСТАЛАХ.
Реальные кристаллы обладают рядом нарушений идеальной структуры, которые называются дефектами кристаллов:
а) точечные дефекты
дефекты Шотки (незанятые частицами узлы);
дефекты Френкеля (смещение частиц из узлов в междуузлия);
примеси (внедренные чужеродные атомы);
б) линейные – дислокации краевые и винтовые локальные нарушения в регулярности расположения частиц, из-за недостроенности отдельных атомных плоскостей, или в последовательности их застройки;
в) плоскостные – границы между зеркалами, ряды линейных дислокаций.
АМОРФНЫЕ ТВЕРДЫЕ ТЕЛА.
Аморфные твердые тела по многим своим свойствам и главным образом по микроструктуре следует рассматривать как сильно переохлажденные жидкости с очень высоким коэффициентом вязкости. С энергетической точки зрения различие между кристаллическими и аморфными твердыми телами хорошо прослеживаются в процессе отвердевания и плавления. Кристаллические тела имеют точку плавления – температуру, когда вещество устойчиво существует в двух фазах – твердой и жидкой (рис1). Переход молекулы твердого тела в жидкость означает, что она приобретает дополнительно три степени свободы поступательного движения. Т.о. единица массы вещества при Т пл. в жидкой фазе имеет большую внутреннюю энергию, чем такая же масса в твердой фазе. Кроме того, меняется расстояние между частицами. Поэтому в целом количество теплоты необходимое для превращения единицы массы кристалла в жидкость будет:
λ = (U ж -U k) + P (V ж -V k),
где λ – удельная теплота плавления (кристаллизации), (U ж -U k) – разность внутренних энергий жидкой и кристаллической фаз, Р – внешнее давление, (V ж -V k) – разность удельных объемов. Согласно уравнению Клайперона - Клаузиуса температура плавления зависит от давления:
 .
.
Видно,
что если (V ж -V k)>
0, то
 >
0, т.е. с ростом давления температура
плавления повышается. Если же объем
вещества при плавлении уменьшается
(V ж -V k)<
0 (вода, висмут), то рост давления приводит
к понижению Т пл.
>
0, т.е. с ростом давления температура
плавления повышается. Если же объем
вещества при плавлении уменьшается
(V ж -V k)<
0 (вода, висмут), то рост давления приводит
к понижению Т пл.
У аморфных тел теплота плавления отсутствует. Нагревание приводит к постепенному увеличению скорости теплового движения и уменьшению вязкости. На графике процесса имеется точка перегиба, которую условно называют температурой размягчения.
Введение
Фазовые диаграммы состояний являются неотъемлемой частью любого обсуждения свойств материалов в тех случаях, когда речь идет о взаимодействии различных материалов. Особенно фазовые диаграммы состояния важны в микроэлектронике, т.к. для изготовления выводов и пассивирующих слоев там приходится использовать большой набор различных материалов. В производстве интегральных микросхем в тесном контакте с различными металлами находится кремний, особое внимание уделим тем фазовым диаграммам, в которых в качестве одной из компонент фигурирует именно кремний.
В данном реферате рассмотрено какие бывают типы фазовых диаграмм, понятие фазового перехода, твердой растворимости, самые важные системы веществ для микроэлектроники.
Типы фазовых диаграмм
Однофазовые диаграммы состояний - это графики, на которых в зависимости от давления, объем и температуры изображают фазовое состояние только одного материала. Обычно не принято рисовать трехмерный график на двумерной плоскости - изображают его проекцию на плоскость температура - давление. Пример однофазной диаграммы состояний дан на рис. 1.
Рис. 1.
На диаграмме четко разграничены области, в которых материал может существовать только в одном фазовом состоянии - как твердое тело, жидкость или газ. Вдоль разграниченных линий вещество может иметь два фазовых состояния (две фазы), находящихся в контексте друг с другом. Имеет место любая из комбинаций: твердое тело - жидкость, твердое тело - пар, жидкость - пар. В точке пересечения линий диаграммы, так называемой тройной точке, могут одновременно существовать все три фазы. Причем это возможно при одной-единственной температуре, поэтому тройная точка служит хорошей точкой отсчета температур. Обычно в качестве точки отсчета выступает тройная точка воды (например, в прецизионных измерениях с использованием термопар, где опорный спай контактирует с системой лед - вода - пар).
Двойная фазовая диаграмма (диаграмма состояния двойной системы) представляет состояние системы с двумя компонентами. На таких диаграммах по оси ординат откладывается температура, по оси абсцисс - процентное соотношение компонент смеси (обычно это или процент от общей массы (вес. %), или процент от общего числа атомов (ат. %)). Давление обычно полагается равным 1 атм. Если рассматривается жидкая и твердая фазы, измерением объема пренебрегают. На рис. 2. представлена типичная двухфазная диаграмма состояний для компонент A и B с использованием весового или атомного процента.

Рис. 2.
Буквой? обозначена фаза вещества A с растворенным веществом B, ? означает фазу вещества B с растворенным в нем веществом A, а? + ? означает смесь этих фаз. Буква (от liquid - жидкий) означает жидкую фазу, а L+?? и L+? означают жидкую фазу плюс фаза или соответственно. Линии, разделяющие фазы, т. е. линии, на которых могут существовать различные фазы вещества, имеют следующие названия: солидус - линия, на которой одновременно существуют фазы? или? с фазами L+? и L+? соответственно; сольвус - линия, на которой одновременно сосуществуют фазы? и? + ? или? и? + ?, и ликвидус - линия, на которой одновременно существует фаза L с фазой L+? или L+?.
Точка пересечения двух линий ликвидуса часто является точкой наименьшей температуры плавления для всех возможных комбинаций веществ A и B и называется эвтектической точкой. Смесь с соотношением компонент в эвтектической точке называется эвтектической смесью (или просто эвтектикой).
Рассмотрим как происходит переход смеси из жидкого состояния (расплава) в твердое и как фазовая диаграмма помогает предсказать равновесную композицию всех фаз, существующих при данной температуре. Обратимся к рис. 3.

Рис. 3.
Предположим, что вначале смесь имела состав C M при температуре T 1 , при температуре от T 1 до T 2 существует жидкая фаза, а при температуре T 2 одновременно существуют фазы L и?. Состав присутствующей фазы L есть C М, состав фазы? есть C ?1 . При дальнейшем снижении температуры до T 3 состав жидкой меняется вдоль кривой ликвидуса, а состав фазы? - вдоль кривой солидуса до пересечения с изотермой (горизонтальной линией) T 3 . Теперь состав фазы L есть C L , а состав фазы есть C ?2 . Следует отметить, что состав C ?2 должен иметь не только вещество, перешедшее в фазу при? при температуре T 3 , но и все вещество, перешедшее в фазу? при более высокой температуре, должно иметь состав C ?2 . Это выравнивание составов должно произойти путем твердотельной диффузии компонента A в существующую фазу?, так что к моменту достижения температуры T 3 все вещество, находящееся в фазе?, будет иметь состав C ?2 . Дальнейшее снижение температуры приводит нас в эвтектическую точку. В ней фазы? и? существуют одновременно с жидкой фазой. При более низких температурах существуют только фазы? и?. Образуется смесь фаз? и? состава C E с агрегатами? с начальным составом C ?3 . Затем, выдерживая эту смесь длительное время при температуре ниже эвтектической, можно получить твердое тело. Образовавшееся твердое тело будет состоять из двух фаз. Состав каждой из фаз можно определить в точке пересечения изотермы с соответствующей линией сольвуса.
Только что было показано, как определить состав каждой из присутствующих фаз. Теперь рассмотрим задачу определения количества вещества в каждой фазе. Во избежания путаницы на рис. 4. еще раз приводится простая двухфазная диаграмма. Предположим, что при температуре T 1 состав расплава есть C M (имеется в виду компонента B), тогда при T 2 фаза L имеет состав C L , а фаза? будет иметь состав C s . Пусть M L - масса вещества, находящегося в твердом состоянии, а M S - масса вещества, находящегося в твердом состоянии. Условие сохранения суммарной массы приводит к следующему уравнению
(M L + M S)C M = M L C L + M S C S .

Рис. 4.
В нем нашел отражение тот факт, что общая масса вещества при температуре T 1 , умноженная на процент B, - есть общая масса вещества B. Она равна сумме масс вещества B, существующего в жидкой и в твердой фазах при температуре T 2 . Решая это уравнение, получаем
Это выражение известно как «правило уровня». С помощью этого правила, зная начальный состав расплава и общую его массу, можно определить массы обеих фаз и количество вещества B в любой фазе для любого участка двухфазной диаграммы. Точно так же можно вычислить и
На рис. 5. приведен еще одни пример отвердения расплава. Снижение температуры от T 1 до T 2 приводит к смешиванию фаз L и? с составом соответственно C M и C ? . По мере дальнейшего охлаждения состав L меняется вдоль ликвидуса, а состав? - вдоль солидуса, как было описано ранее. При достижении температуры T 3 состав? станет равным C М, и, как следует из правила уровня, при температуре, меньшей T 3 , жидкая фаза существовать не может. При температуре, меньшей T 4 , фазы? и? существуют как агрегаты фаз? и?. Например, при температуре T 5 агрегаты фазы? будут иметь состав, определяемый пересечением изотермы T 5 и сольвуса?. Состав? определяется аналогично - пересечением изотермы и сольвуса?.

Рис. 5.
Участки двухфазной диаграммы, называемые до сих пор? и?, - это участки твердой растворимости: в области? растворено A и B. Максимальное количество A, которое может быть растворено в B при данной температуре, находятся в зависимости от температуры. При эвтектической или более высокой температуре может иметь место быстрое сплавливание A и B. Если полученный при этом сплав резко охладить, то атомы A могут быть «пойманы» в решетке B. Но если твердая растворимость при комнатной температуре намного ниже (это говорит о том, что при этой температуре рассматриваемый подход не слишком пригоден), то в сплаве могут возникать сильнейшие напряжения, существенно влияющие на его свойства (при наличии значительных напряжений возникают пересыщенные твердые растворы, и система находится не в равновесном состоянии, а диаграмма дает информацию только о равновесных состояниях). Иногда, такой эффект является желательным, например при упрочнении стали закалкой с получением мартенсита. Но в микроэлектронике его результат будет разрушительным. Поэтому легирование, т. е. внесение добавок в кремний до диффузии, проводится при повышенных температурах с таким расчетом, чтобы предупредить повреждение поверхности из-за избыточного сплавления. Если же количество легирующей примеси в подложке окажется выше предела твердой растворимости при любой температуре, то появляется вторая фаза и связанная с ней деформация.
Таким образом, выражение (16.14) должно определять истинное равновесное давление пара при заданной температуре. Так как и являются функциями от давления и температуры соответствующих фаз, (16.14) является уравнением линии перехода между двумя фазами. Таким образом уравнение линии перехода, например кривой давления пара или кривой плавления, представляет собой соотношение между и Поэтому наилучшим способом изображения различных фаз является -диаграмма, На фиг. 29 показана обычная -диаграмма. Кривая давления пара разделяет газовую и жидкую фазы, а кривая плавления - жидкую и твердую фазы.
Кривая давления пара оканчивается в критической точке К. При температурах выше критической газ и жидкость непрерывно переходят друг в друга без поглощения или отдачи тепла и без скачкообразного изменения плотности, что имеет место в случае, например, испарения. Неоднократно делались попытки найти аналогичную «критическую» точку в конце кривой плавления, но даже при очень высоких давлениях такой точки не обнаружено.
При понижении температуры давление пара уменьшается. Но при этом уменьшается и давление, при котором кристаллизуется жидкость (давление плавления). При определенной температуре давление пара становится равным давлению плавления кристалла (точка на фиг. 29). При этих температуре и давлении газовая, жидкая и твердая (кристаллическая) фазы могут сушествовать в равновесии между собой; называется тройной точкой. Ниже этих температуры и давления газ может прямо переходить в твердую фазу, а твердая фаза возгоняться (сублимироваться); соответствующая линия перехода называется иногда кривой сублимации (или кривой возгонки).

Фиг. 29. -диаграмма.
Обычно температура плавления повышается с увеличением давления, поэтому кривая плавления на диаграмме наклонена вправо. Однако в некоторых случаях температура плавления понижается с увеличением давления, например для воды между О и 2000 атм (фиг. 30). Точка плавления воды, т. е. температура плавления при давлении 1 атм, по определению равна 0° С. Тройная точка лежит немного выше; ее координаты 0,007 С и 4,6 мм рт. ст.
На примере воды видно, что фазовая диаграмма не всегда имеет такой простой характер, как показано На фиг. 29. Вода может существовать в виде нескольких твердых фаз, которые различаются своей кристаллической структурой. Фазовая диаграмма гелия (фиг. 31) стоит особняком и отличается от других диаграмм отсутствием кривой сублимации: жидкая зона распространяется до абсолютного нуля. Вместо тройной точки мы имеем в этом случае так называемую -кривую, которая разделяет две различные зоны, обычно обозначаемые римскими цифрами

Фиг. 30. -диаграмма воды.
Переход между двумя жидмими фазами I и II проявляется не в скачкообразном изменении плотности и не в наличии теплоты перехода, как это имеет место при обычных переходах (плавлении, конденсации и сублимации), а в резком изменении коэффициента теплового расширения, сжимаемости и удельной теплоемкости, т. е. производных основных термодинамических величин. Эти переходы часто называют переходами второго рода
Из уравнения (16.14) линии перехода двух фаз мы можем вывести соотношение между различными
характеристическими термодинамическими величинами линии перехода. Рассмотрим точку на линии перехода (фиг. 32); в этой точке Если теперь увеличить температуру на и давление на таким образом, чтобы остаться на линии перехода, мы придем в точку в которой обе фазы снова находятся в равновесии.

Фиг. -диаграмма гелия.
Таким образом, если есть увеличение термодинамического потенциала для фазы 1 и - его увеличение для фазы 2, то мы имеем
Сравнивая с (16.14), мы видим, что
![]()
где есть малое увеличение термодинамического потенциала фазы 1 или 2 вдоль линии перехода.
Согласно § 13, термодинамический потенциал равен свободной энтальпии одного киломоля, откуда, учитывая (13.3), мы получаем
где - малые приращения вдоль линии перехода и - энтропии и объемы одного киломоля каждой фазы вдоль линии перехода. Выражение (16.17) можно переписать в виде
![]()

Фиг. 32. К выводу уравнения Клайперона-Клаузиуса.
Так как во время перехода температура остается постоянной, разность энтропий между двумя фазами равна теплоте перехода, деленной на температуру, откуда, наконец, получаем так называемое уравнение Клаузиуса - Клайперона
![]()
Из этого уравнения вытекает ряд важных следствий. Если мы, например, повышаем температуру и приближаемся к критической точке вдоль кривой давления пара, то разность плотностей пара и жидкости, а следовательно, разность удельных объемов в знаменателе уравнения (16.19) непрерывно уменьшается. Но крутизна кривой давления пара на p-T-диаграмме, как показывает опыт, не становится бесконечной в критической точке. Следовательно, на основании (16.19) мы можем сделать вывод, что по мере приближения к критической точке теплота испарения непрерывно уменьшается и, наконец, становится равной нулю. Это согласуется с опытными данными.
Из уравнения (16.19) следует также, что величина положительна, если молярный объем второй фазы больше объема первой фазы и если для осуществления перехода из первой фазы во вторую к системе необходимо подводить тепло. Это также согласуется с формой различных линий перехода, полученных экспериментально. Следует отметить, что крутизна кривой
плавления воды отрицательна, несмотря на то что величина положительна. Уравнение (16.19) показывает, что в этом случае объем второй фазы (воды) должен быть меньше объема первой фазы (льда), тогда как обычно твердая фаза имеет меньший молярный объем. Эти особые свойства воды уже давно известны из опыта.

Рассмотрим P − T − X диаграммы для бинарных систем. Интенсивные работы по изучению P − T − X диаграмм состояния показали, что использование высоких давлений (десятки и сотни тысяч атмосфер) в ряде случаев приводит к изменению типа диаграммы состояния, к резкому изменению температур фазовых и полиморфных превращений, к появлению новых фаз, отсутствующих в данной системе при атмосферном давлении. Так, например, диаграмма с неограниченной растворимостью в твердом состоянии при высоких температурах и распадом твердого раствора α на два твердых раствора α1 + α2 при низких температурах может с увеличением давления постепенно переходить в диаграмму с эвтектикой (см. рис. 4.18,а ). На рис. 4.18,б показана диаграмма состояния системы Ga–P, в которой образуется полупроводниковое соединение GaP. В зависимости от давления это соединение может плавиться конгруэнтно или инконгруэнтно. Соответственно изменяется и вид двойной диаграммы T − X на различных изобарических сечениях тройной P − T − X диаграммы.
На практике объемные P − T − X диаграммы строятся очень редко. Обычно фазовые превращения в трехмерных P − T − X диаграммах ана
Рис. 4.18. а - P − T − X диаграмма; б - P − T − X диаграмма состояния
системы Ga–P с конгруэнтно и инконгруэнтно плавящимся соединением GaP в
зависимости от давления.
лизируют с помощью их проекций на плоскости P − T , T − X и P − X , а также различных сечений при постоянных значениях температуры или давления (см. рис. 4.18,а ).
Заметим, что при анализе фазовых превращений в системе следует различать P − T − X фазовые диаграммы, в которых давление диссоциации P дис9 мало и P на фазовой диаграмме - это внешнее давление и в которых давление диссоциации велико и P - это P дис. В системах, компоненты которых обладают низким давлением диссоциации и в которых максимальная температура плавления смеси ниже самой низкой температуры кипения (в системе нет легколетучих компонентов), ролью газовой фазы при фазовых превращениях можно пренебречь. Если же давление диссоциации какого-либо из компонентов велико (система содержит легколетучие компоненты), то состав газовой фазы необходимо учитывать при температурах как выше, так и ниже ликвидуса.
Рассмотрим подробнее фазовые диаграммы P дис − T − X с высоким
давлением диссоциации (фазовые диаграммы с легколетучими компонентами). Следует отметить, что внимание к ним повысилось в связи с возросшей ролью в полупроводниковой электронике соединений, содержащих летучие компоненты. Например, к ним относятся соединения AIIIBV, содержащие легколетучие компоненты фосфор и мышьяк, соединения AIIBVI, содержащие ртуть, AIVBVI, содержащие серу, и т. д.
Все полупроводниковые соединения обладают более или менее протяженной областью гомогенности, то есть способны растворять в себе
9 P дис - равновесное для данных условий давление диссоциации всех фаз, находящихся в равновесии. При наличии в системе одного легколетучего компонента P дис - это равновесное давление диссоциации легколетучего компонента системы.
какой-либо из компонентов сверх стехиометрического состава или третий компонент.
Любые отклонения от стехиометрического состава сказываются на электрических свойствах (см. гл. 3). Поэтому для воспроизводимого получения кристаллов, содержащих летучий компонент, с заданными свойствами необходимо и воспроизводимое получение соединений заданного состава.
Однако летучесть одного их компонентов соединения приводит к отклонению от стехиометрического состава из-за образования вакансий - анионных или катионных - в зависимости от того, давление диссоциации какого компонента будет выше, и, соответственно, избытка другого компонента. Как уже обсуждалось в гл. 3, вакансии в ряде соединений могут создавать акцепторные или донорные уровни, тем самым влияя на физические свойства.
Энергия образования вакансий в позициях A и B практически никогда не бывает одинаковой, поэтому концентрация анионных и катионных вакансий также различна, а область гомогенности соединения оказывается несимметричной относительно стехиометрического состава. Соответственно практически для всех соединений максимум температуры плавления не соответствует сплаву стехиометрического состава.10
Предотвратить изменение состава соединения за счет летучести можно, если выращивать его из расплава или раствора при внешнем давлении летучего компонента, равном давлению диссоциации при температуре выращивания. Это условие и выбирают с помощью P дис − T – X диаграмм.
Давление диссоциации легколетучего компонента в сплавах сильно зависит от его состава, как правило, понижаясь с уменьшением концентрации этого компонента, как, например, для системы In–As (давление диссоциации мышьяка понижается почти на четыре порядка с уменьшением концентрации мышьяка в интервале от 100 до 20% ). В результате давление диссоциации летучего компонента в соединении оказывается намного меньше давления диссоциации над чистым компонентом при той же температуре.
Это обстоятельство используется в двухтемпературной схеме получения этого соединения. В одной печи создаются две температурные зоны.
10Тем не менее, для соединений, в частности AIII BV , с узкой областью гомогенности и большинства соединений, в частности AIV BVI , со средней шириной области гомогенности применяется понятие конгруэнтно плавящихся соединений, так как отклонения реальной температуры плавления соединения от температуры плавления соединения стехиометрического состава незначительны.

Рис. 4.19. P дис − T сечение P дис − T − X диаграммы состояния системы Pb–S. 1 -
трехфазная линия; 2 - PS 2 чистой серы над PbS+S2 ; 3 - PS 2 над PbS+Pb.
Одна имеет температуру T 1, равную температуре кристаллизации соединения. Здесь помещают контейнер с расплавом. Во второй зоне помещают чистый летучий компонент соединения - As. Температура T 2 во второй зоне поддерживается равной температуре, при которой давление диссоциации летучего компонента в чистом виде равно давлению диссоциации этого компонента в соединении при температуре T 1. В результате в первой зоне давление паров летучего компонента над соединением равно его парциальному давлению диссоциации в соединении, что предотвращает улетучивание этого компонента из расплава и обеспечивает кристаллизацию соединения заданного состава.
На рис. 4.19 приведена P − T проекция фазовой диаграммы Pb–S.
Сплошной линией показана линия трехфазного равновесия твердой, жидкой и газообразной фаз, ограничивающая область устойчивости твердого соединения; пунктиром - изоконцентрационные линии в пределах области гомогенности. Изоконцентрационные линии показывают составы с равным отклонением от стехиометрии (одинаковые составы) в сторону избытка свинца (проводимость n -типа) или в сторону избытка серы (проводимость p -типа), равновесные при данных значениях температуры и давления паров серы. Линия n = p соответствует значениям температуры и давления PS 2 , при которых твердая фаза имеет строго стехиометрический состав. Она пересекает трехфазную линию при температуре, которая является температурой плавления соединения стехиометрического состава. или в сторону избытка серы (проводимость p -типа) .
Как видно из рис. 4.19, температура плавления соединения стехиометрического состава ниже максимальной температуры плавления, которую имеет сплав с избытком свинца по сравнению с формульным составом. Видна резкая зависимость состава кристалла от парциального давления паров летучего компонента. В области высоких температур все кривые, соответствующие разным составам, приближаются к линии n = p . С понижением температуры разница между равновесными давлениями, соответствующими разным составам, увеличивается. Этим объясняется трудность получения сплава заданного состава непосредственно при кристаллизации, проходящей при высоких температурах. Поскольку кривые парциального давления для разных составов близки, небольшие случайные отклонения давления паров летучего компонента могут привести к ощутимому изменению состава твердой фазы.
Если же кристалл после выращивания подвергнуть длительному отжигу при более низких температурах и таком давлении, что изоконцентрационные линии для разных составов резко расходятся, то состав кристалла можно довести до заданного. Этим часто пользуются на практике.